Tabela periódica: como ela surgiu e por que é tão importante?
Imprescindível para os estudos de Química, esse instrumento já tem mais de 150 anos. Mesmo assim, podemos dizer que seu processo de montagem, provavelmente, ainda não terminou

Acessibilidade
A tabela periódica dispõe os elementos químicos de maneira sistemática, organizando-os a partir de suas propriedades e estrutura atômica. Mas qual é a sua origem e quem foi o responsável por idealizá-la? Por que ela é tão importante? Neste artigo, tratamos deste tema, que sempre aparece no Exame Nacional do Ensino Médio (Enem) e vestibulares em geral.
NAVEGUE PELOS CONTEÚDOS
O que é a tabela periódica? Conheça a história
Compreender os inúmeros elementos químicos descobertos, assim como suas aplicações, fez parte de uma busca incessante para muitos cientistas no século 19.
Diante da falta de informações, os pesquisadores empreenderam esforços para encontrar padrões e generalizações nesse vasto conjunto de propriedades. A questão central era: como sistematizar e organizar todo esse conhecimento de maneira coerente?
Para encontrar uma resposta, estudiosos notáveis precisaram se dedicar, como Johann Dobereiner, Alexandre Emile Beguyer de Chancoutois, John Alexander Reina Newlands, Dmitri Ivanovich Mendeleiev e Henry G. J. Moseley.
Com base em sua imaginação, intuição e profundo conhecimento, eles propuseram organizar os elementos químicos de acordo com as propriedades de cada um, considerando suas atividades e conhecimentos pessoais para fazer isso.
Quem criou a tabela periódica?
Muitas pessoas estiveram envolvidas na história da tabela periódica:
- Johann Dobereiner propôs a Lei das tríades, que organizou os elementos em grupos de três. Dobereiner estabeleceu uma relação específica entre as massas atômicas e as propriedades químicas semelhantes dos elementos.
- Alexandre Emile Beguyer de Chancoutois examinou os elementos químicos conhecidos até a data 1862, organizando-os ao redor de um cilindro e na ordem crescente de massa atômica. Ele observou que as propriedades químicas apresentavam repetição a cada sete elementos.
- John Alexander Reina Newlands é responsável pela Lei das oitavas, na qual um elemento químico apresenta comportamento análogo ao oitavo elemento seguinte. A lei faz uma analogia aos sete intervalos da escala musical.
- Dmitri Ivanovich Mendeleiev organizou os elementos em ordem crescente de peso atômico e percebeu a repetição periódica das propriedades. Por essa razão, chamou sua descoberta de Tabela periódica dos elementos.

Inicialmente, Dmitri se aprofundou no estudo das línguas mortas, como latim e grego. Mas, após um primeiro contato com a Ciência, revelou todo o seu potencial. Mendeleiev colaborou com renomados cientistas da época, como Bunsen, Canizarro e Kirchhoff, dos quais obteve valiosas informações sobre os novos elementos químicos em descoberta.

- Henry G. J. Moseley constatou que a raiz quadrada da frequência dos raios X emitidos pelos núcleos era proporcional ao número atômico (Z). Com base nesses dados, ele sugeriu que o número atômico representava a quantidade de prótons no núcleo do átomo de um elemento químico. Por volta de 1920, James Chadwick confirmou essa hipótese. Hoje, a tabela periódica é organizada em ordem crescente de número atômico.
Organização da tabela periódica
A tabela periódica atual exibe divisões claramente definidas em linhas horizontais e verticais. Os elementos químicos, organizados em ordem crescente de número atômico ao longo de uma linha horizontal, são denominados períodos; quando observados em linhas verticais, usamos os termos famílias, grupos ou colunas.
Períodos
Os períodos da tabela periódica são as linhas horizontais que organizam os elementos químicos de acordo com seu número atômico crescente. Cada período tem início com o elemento de menor número atômico e se encerra com o elemento de maior número atômico naquela linha específica.
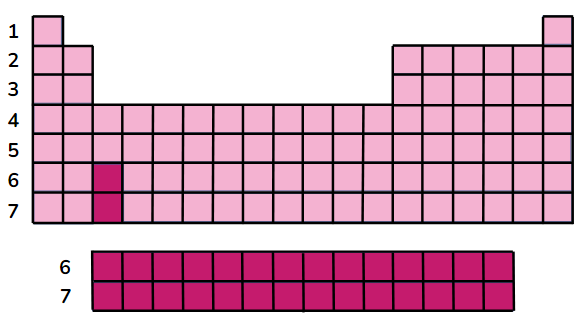
Embora os elementos dentro de um período compartilhem o mesmo nível de energia principal, eles podem variar nos subníveis de energia (s, p, d, f):
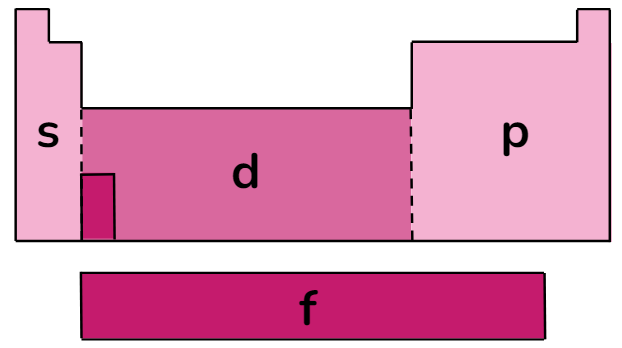
Famílias ou grupos
As famílias ou os grupos na tabela periódica são as colunas verticais que organizam os elementos químicos com base em suas propriedades similares. Cada coluna representa uma família, e os elementos dentro de uma mesma família compartilham características químicas e comportamentos semelhantes.
Na tabela periódica há 18 grupos numerados de 1 a 18:
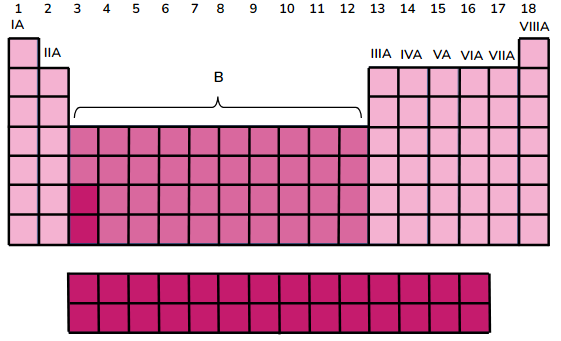
Os elementos em um grupo compartilham o mesmo número de elétrons na camada externa, o que influencia significativamente seu comportamento químico. Por exemplo: os elementos do Grupo 1, conhecidos como metais alcalinos, possuem um elétron na camada externa, já os elementos do Grupo 18, chamados de gases nobres, têm uma camada externa completa.
Além da numeração, as famílias podem receber o nome do primeiro elemento químico ou nomes específicos, como:
1. Metais alcalinos (exceto o hidrogênio);
2. Metais alcalino-terrosos;
3-12. Metais de transição;
13. Família do boro;
14. Família do carbono;
15. Família do nitrogênio;
16. Família do oxigênio, ou calcogênios;
17. Família do flúor, ou halogênios;
18. Gases nobres.
Existe ainda uma última classificação, que pode se dividir em metais, não metais (ametais), gases nobres e hidrogênio.
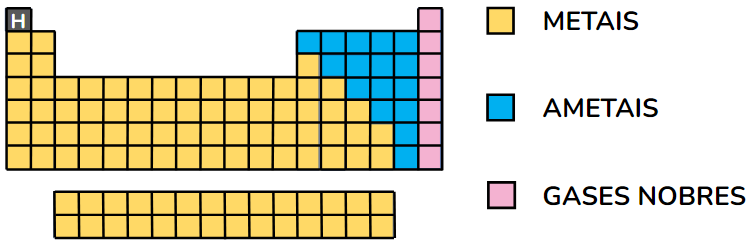
Metais
- São bons condutores de corrente elétrica e de calor;
- Apresentam brilho característico;
- São transformados em lâminas (maleáveis) e também em fios (dúcteis);
- São sólidos nas condições ambientais (25 °C e 1 atm, exceto o mercúrio);
- Tendência de formar cátions. Transformação física, fusão, do metal Gálio.
Não metais ou ametais
- Constituem grupo de 15 elementos (B, C, N, Si, P, O, S, Se, F, Cl, As, Br, Te, I e At), que apresentam a tendência de formar ânions;
- Não são bons condutores de corrente elétrica e de calor;
- Não possuem brilho característico.
Gases nobres
- São formados por seis 6 elementos químicos (família 18);
- Inertes quimicamente, raros e os únicos encontrados na natureza na forma de átomos;
- Usados em letreiros luminosos.
Hidrogênio
- Destaque para as características exclusivas do elemento químico H. Por mais que esteja no lado esquerdo da tabela periódica, acima do lítio, não tem características de metais alcalinos;
- Está na natureza em forma de gás hidrogênio H2(g).
Séries especiais
Na tabela periódica, as séries especiais são agrupamentos específicos de elementos que compartilham propriedades semelhantes ou manifestam comportamentos distintos.
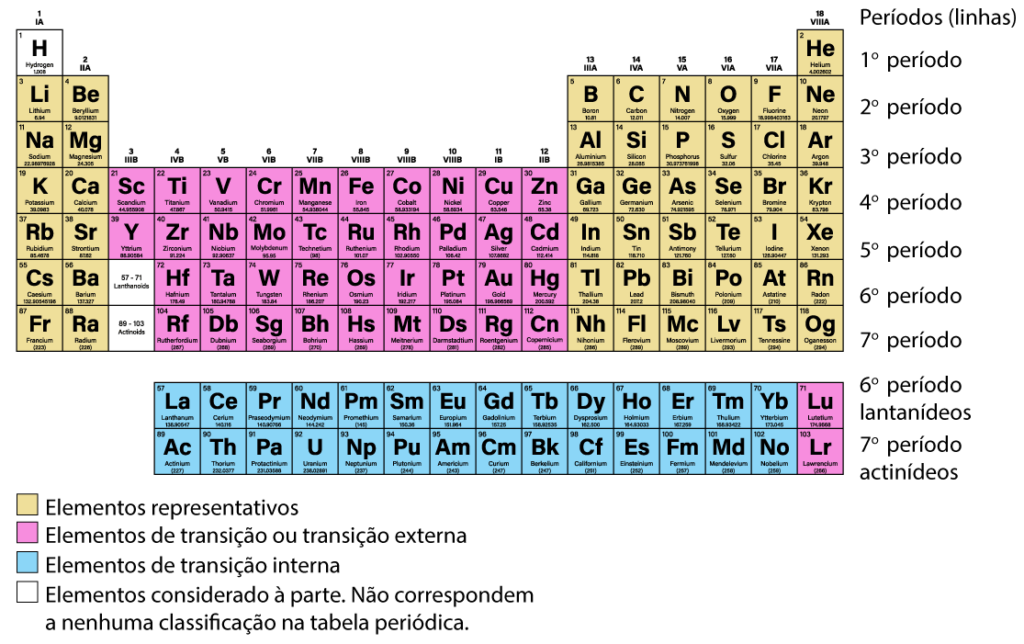
Elementos representativos
Os elementos representativos estão presentes nos grupos 1 e 2 (metais alcalinos e alcalino-terrosos) e nos grupos 13 a 18 (blocos s e p). Eles exibem, em geral, propriedades químicas semelhantes, com o mesmo número de elétrons na camada mais externa, resultando em configurações eletrônicas similares.
Elementos de transição
Os elementos de transição ocupam os blocos d da tabela periódica, que abrangem os grupos 3 a 12. Demonstram propriedades metálicas, tais como condutividade elétrica, maleabilidade e ductilidade. À medida que se percorre um período na tabela periódica, as propriedades desses elementos mudam gradativamente devido ao preenchimento sequencial dos orbitais d.
Gases nobres
Os gases nobres estão no grupo 18 da tabela periódica. Reconhecidos por sua estabilidade e baixa reatividade, possuem uma camada de valência completa que confere estabilidade energética, tornando-os menos propensos a formar ligações químicas.
Série dos lantanídeos
Estão no bloco f entre os grupos 3 e 12, os elementos da série dos lantanídeos exibem propriedades químicas e físicas semelhantes. São comumente denominados "metais de transição interna" devido à sua posição na tabela periódica.
Série dos actinídeos
Os actinídeos ficam no bloco f, abaixo dos lantanídeos, e compartilham características semelhantes com os lantanídeos, com uma variação gradual ao longo da série. Conhecidos também como "metais de transição interna", incluem muitos elementos radioativos, sendo o actínio (Ac) o primeiro elemento transurânico descoberto.
👉 Leia também:
Conheça os principais tipos de cadeias carbônicas
Catalisadores: o que são e exemplos de como funcionam
Conheça as propriedades dos compostos orgânicos
Propriedades periódicas: o que e quais são?
Na tabela periódica, os elementos são dispostos de acordo com suas propriedades, proporcionando uma compreensão mais fácil das características dos átomos e de seus compostos. Vamos analisar algumas das propriedades fundamentais presentes na tabela periódica.
Raio atômico
O raio atômico é a medida que quantifica o tamanho do átomo. Na tabela periódica, observa-se que o raio atômico cresce ao longo de um período (linha) da esquerda para a direita, e ao longo de um grupo (coluna) de cima para baixo, o que se deve à adição de camadas de elétrons.
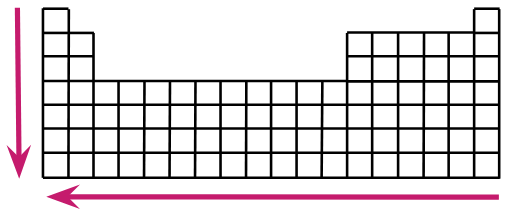
Energia de ionização
A energia de ionização representa a energia necessária para retirar um elétron de um átomo neutro. Ela aumenta, ao longo de um período (linha), da esquerda para a direita e de baixo para cima, em um grupo (coluna) na tabela periódica.
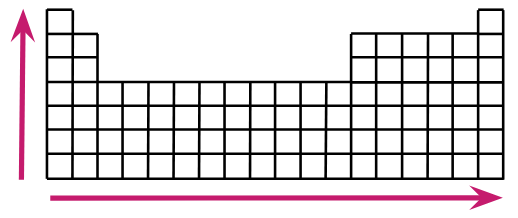
Afinidade eletrônica
A afinidade eletrônica é a medida da facilidade com que um átomo adquire um elétron. Similar à energia de ionização, a afinidade eletrônica aumenta, ao longo de um período (linha), da esquerda para a direita e de baixo para cima, em um grupo (coluna) na tabela periódica.
Eletronegatividade
A eletronegatividade refere-se à capacidade de um átomo atrair elétrons quando participa de uma ligação química. Esta propriedade segue padrões semelhantes aos da energia de ionização e afinidade eletrônica na tabela periódica.
Eletropositividade
A eletropositividade é uma característica química que indica a propensão de um átomo em ceder elétrons durante a formação de ligações químicas. Observa-se um aumento da eletropositividade de cima para baixo em um grupo e da direita para a esquerda em um período.
Densidade
A densidade representa a relação entre a massa de um elemento e o volume ocupado por ele. Observa-se um aumento na densidade ao longo de uma mesma família, de cima para baixo, e um aumento progressivo em direção ao ósmio ao longo do mesmo período.Parte superior do formulário
Pontos de fusão e ebulição
Os pontos de fusão e ebulição representam as temperaturas nas quais um elemento passa de um estado para outro. Esses valores apresentam variações substanciais na tabela periódica, sendo impactados por uma série de fatores, incluindo a estrutura cristalina e a intensidade das forças intermoleculares.
A importância da tabela periódica
Uma das principais funcionalidades da tabela periódica é a possibilidade de prever para que serve cada elemento químico e quais compostos irão resultar nas suas combinações.
Isso só acontece porque os elementos são agrupados não apenas por seus números atômicos e em ordem crescente, mas também segundo a distribuição eletrônica de cada um, ou seja, a quantidade de elétrons na camada de valência.
Outros motivos que fazem a tabela periódica ser tão importante incluem:
- Descoberta de novos elementos
Com base nas propriedades de elementos vizinhos na tabela, os cientistas podem estimar as propriedades prováveis de novos elementos antes mesmo deles serem produzidos em laboratório; - Referência para informação
A tabela periódica é uma referência valiosa para estudantes, cientistas e profissionais da área, fornecendo informações essenciais sobre cada elemento, como símbolo, número atômico, massa atômica e configuração eletrônica; - Compreensão da estrutura atômica
Ajuda a entender a organização dos elétrons em órbitas ao redor do núcleo do átomo. Ela mostra como os elétrons estão distribuídos em camadas e subníveis, contribuindo para a compreensão das propriedades químicas e da ligação entre átomos; - Educação e pesquisa:
A tabela periódica é uma ferramenta educacional essencial, introduzindo os conceitos fundamentais da química aos alunos e servindo como base para pesquisas científicas em diversas áreas, como Química, Física, Engenharia de materiais e outras disciplinas relacionadas.
Curiosidades sobre a tabela periódica
Desde sua criação, a tabela periódica se tornou uma ferramenta essencial para os estudos químicos, ao revelar padrões e conexões entre os elementos. Neste contexto, vamos explorar algumas curiosidades:
Quantos elementos existem na tabela periódica?
A tabela periódica mais recente, adotada pela União Internacional da Química Pura e Aplicada (IUPAC), é composta por 118 elementos químicos, sendo 92 naturais e 26 artificiais.
Qual o elemento mais perigoso da tabela periódica?
Trata-se do Plutônio, descoberto m 1940, com papel fundamental no desenvolvimento das armas nucleares e na produção de energia em reatores nucleares.
Seu envolvimento na Segunda Guerra Mundial é um capítulo sombrio da história, o que evidencia seu poder destrutivo. No entanto, o plutônio é importante para a execução de missões espaciais e alguns tratamentos médicos, exigindo manipulação cuidadosa devido aos riscos que apresenta.
Qual a única letra que não está presente na tabela periódica?
A letra J é a única ausente na tabela periódica. Já houve sugestões para nomes (e símbolos) de elementos que começam com a letra J, mas, por várias razões, eles não estão presentes na versão atual.
Qual o elemento mais pesado da tabela periódica?
O elemento mais pesado da tabela periódica que ocorre naturalmente é o Urânio, com número atômico 92. Elementos mais pesados são sintéticos, e o elemento mais pesado já criado pelo homem é o Oganessônio (Og), com número atômico 118.
Qual elemento possui o nome mais longo na tabela periódica?
O elemento com o nome mais longo na tabela periódica é o Ununpentium, que significa 115 em latim. Mas ele foi renomeado para Moscovium (Mc) em homenagem à cidade de Moscou.
O que o hélio tem de diferente dos outros elementos?
O Hélio é o único elemento que foi descoberto pela primeira vez no Sol antes de ser encontrado na Terra. Ele foi identificado primeiramente em espectros solares antes de ser isolado aqui na Terra.
Quais são os nomes de elementos derivados de países?
Alguns elementos receberam seus nomes em homenagem a países. Por exemplo, o elemento "Polônio" foi nomeado em honra à Polônia, que é a terra natal de Marie Curie, que descobriu o elemento.
Outros exemplos são:
- Americium (Am), que recebeu seu nome em referência aos Estados Unidos da América, onde foi isolado pela primeira vez;
- Einsteinium (Es), que recebeu esse nome em homenagem ao cientista Albert Einstein;
- Darmstádtio (Ds), que homenageia a cidade de Darmstadt, na Alemanha, onde fica o Centro de Pesquisa de Íons Pesados;
- Livermório (Lv), que recebeu esse nome em homenagem ao Laboratório de Radiação de Liverpool, no Reino Unido, por suas contribuições para a pesquisa de elementos pesados.
Qual elemento está mais presente na crosta terrestre?
O elemento mais abundante na crosta terrestre é o oxigênio, compreendendo cerca de 46,6% da massa total da crosta.
O que sabemos sobre a aplicação prática dos elementos?
Todos os elementos na tabela periódica têm aplicações práticas em nossa vida cotidiana, seja na forma de elementos essenciais para a vida, como carbono e oxigênio, ou em produtos industriais, eletrônicos, medicamentos e muito mais.
Resumo: tabela periódica e suas propriedades
Vamos ver se você compreendeu os principais pontos sobre a tabela periódica?
- Dmitri Ivanovich Mendeleiev é reconhecido como o criador da tabela periódica, organizando os elementos com base nas propriedades e no peso atômico;
- A tabela tem sete períodos (linhas horizontais) e 18 grupos (colunas verticais);
- Classificamos os elementos em metais, não metais, gases nobres e hidrogênio, cada grupo com propriedades específicas;
- Raio atômico, energia de ionização, afinidade eletrônica, eletronegatividade, eletropositividade, densidade e pontos de fusão/ebulição são algumas das propriedades periódicas presentes na tabela;
- A tabela periódica mais recente conta com 118 elementos, sendo 92 naturais e 26 artificiais.

Como a tabela periódica cai no Enem e nos vestibulares
As questões relacionadas à tabela periódica geralmente envolvem a compreensão das propriedades dos elementos químicos e sua organização na tabela. No entanto, é fundamental não desviar a atenção de outros conceitos químicos que podem aparecer no Enem e nos vestibulares. Veja alguns exemplos de exercícios:
Exemplo 1
(Espcex Aman 2019) A representação a seguir corresponde à parte superior da tabela periódica, na qual as letras não correspondem aos verdadeiros símbolos dos elementos.
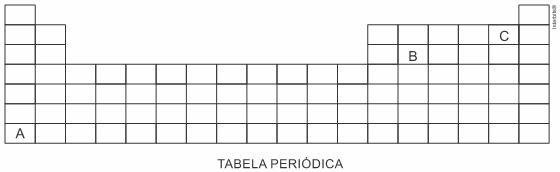
Considere as afirmativas acerca dos elementos hipotéticos (A, B, C) apresentados na tabela periódica.
I. Dentre os elementos hipotéticos, o elemento A é o de maior afinidade eletrônica (“energia liberada quando um átomo isolado, no estado gasoso, captura um elétron”).
USBERCO, João e SALVADOR, Edgard. Química, Vol. 2: Físico-Química. 12ª ed. Reform - São Paulo: Ed. Saraiva, 2009, pág. 202.
II. Dentre os elementos hipotéticos, pode-se afirmar que o elemento B é o de maior eletropositividade (“capacidade de um átomo perder elétrons, originando cátions”).
USBERCO, João e SALVADOR, Edgard. Química, Vol. 2: Físico-Química. 12ª ed. Reform - São Paulo: Ed. Saraiva, 2009, pág. 202.
III. Dentre os elementos hipotéticos, pode-se afirmar que o elemento C é o mais eletronegativo (“força de atração exercida sobre os elétrons de uma ligação”).
USBERCO, João e SALVADOR, Edgard. Química, Vol. 2: Físico-Química. 12ª ed. Reform – São Paulo: Ed. Saraiva, 2009, pág. 202.
Das afirmativas feitas está(ão) correta(s) apenas
a) I.
b) II.
c) III.
d) I e II.
e) II e III.
Resposta: [C]
É preciso destacar que, entre os elementos hipotéticos, é possível afirmar que o elemento C se destaca como o mais eletronegativo, referindo-se à "força de atração exercida sobre os elétrons de uma ligação". Essa característica se deve ao fato de o elemento C possuir o menor número de camadas, que totalizam apenas duas, resultando em um raio atômico mais reduzido.
Exemplo 2
(Enem 2018) Na mitologia grega, Nióbia era a filha de Tântalo, dois personagens conhecidos pelo sofrimento. O elemento químico de número atômico (Z) igual a 41 tem propriedades químicas e físicas tão parecidas com as do elemento de número atômico 73 que chegaram a ser confundidos. Por isso, em homenagem a esses dois personagens da mitologia grega, foi conferido a esses elementos os nomes de nióbio (Z=41) e tântalo (Z=73). Esses dois elementos químicos adquiriram grande importância econômica na metalurgia, na produção de supercondutores e em outras aplicações na indústria de ponta, exatamente pelas propriedades químicas e físicas comuns aos dois.
KEAN, S. A colher que desaparece: e outras histórias reais de loucura, amor e morte a partir dos elementos químicos. Rio de Janeiro: Zahar, 2011 (adaptado).
A importância econômica e tecnológica desses elementos, pela similaridade de suas propriedades químicas e físicas, deve-se a
a) terem elétrons no subnível f.
b) serem elementos de transição interna.
c) pertencerem ao mesmo grupo na tabela periódica.
d) terem seus elétrons mais externos nos níveis 4 e 5, respectivamente.
e) estarem localizados na família dos alcalinos terrosos e alcalinos, respectivamente.
Resposta: [C]
A uniformidade nas propriedades químicas e físicas dos elementos químicos decorre de sua inclusão em um mesmo grupo ou família da tabela periódica. É relevante notar, que tanto o nióbio (Nb; Z = 41) quanto o tântalo (Ta; Z = 73) ocupam a mesma posição no grupo 5, anteriormente denominado como grupo V B, na tabela