Química no Enem 2024: veja os temas que mais aparecem na prova
Quer mandar bem na prova de Ciências da Natureza? Então saiba que Química tem as suas particularidades no Enem. Veja os temas que devem estar no seu radar este ano

Acessibilidade
A Química é uma Ciência Exata cujas áreas estão agrupadas em quatro grandes grupos: química inorgânica, química orgânica, físico-química e química-analítica, sem falar nos temas interdisciplinares, como bioquímica e química-ambiental. Feitas as devidas apresentações, você deve estar se perguntando: com tantos assuntos, o que estudar em Química para o Enem?
No Aprova Total, priorizamos informações completas e assertivas. Por isso, todo ano, atualizamos o relatório que traz a análise de incidência de temas no Exame Nacional do Ensino Médio (Enem) em cada matéria.
Ele é desenvolvido a partir da análise de todas as questões do Enem e seus respectivos conteúdos abordados, reunindo dados desde 2016. Veja o gráfico referente aos assuntos de Química no Enem:
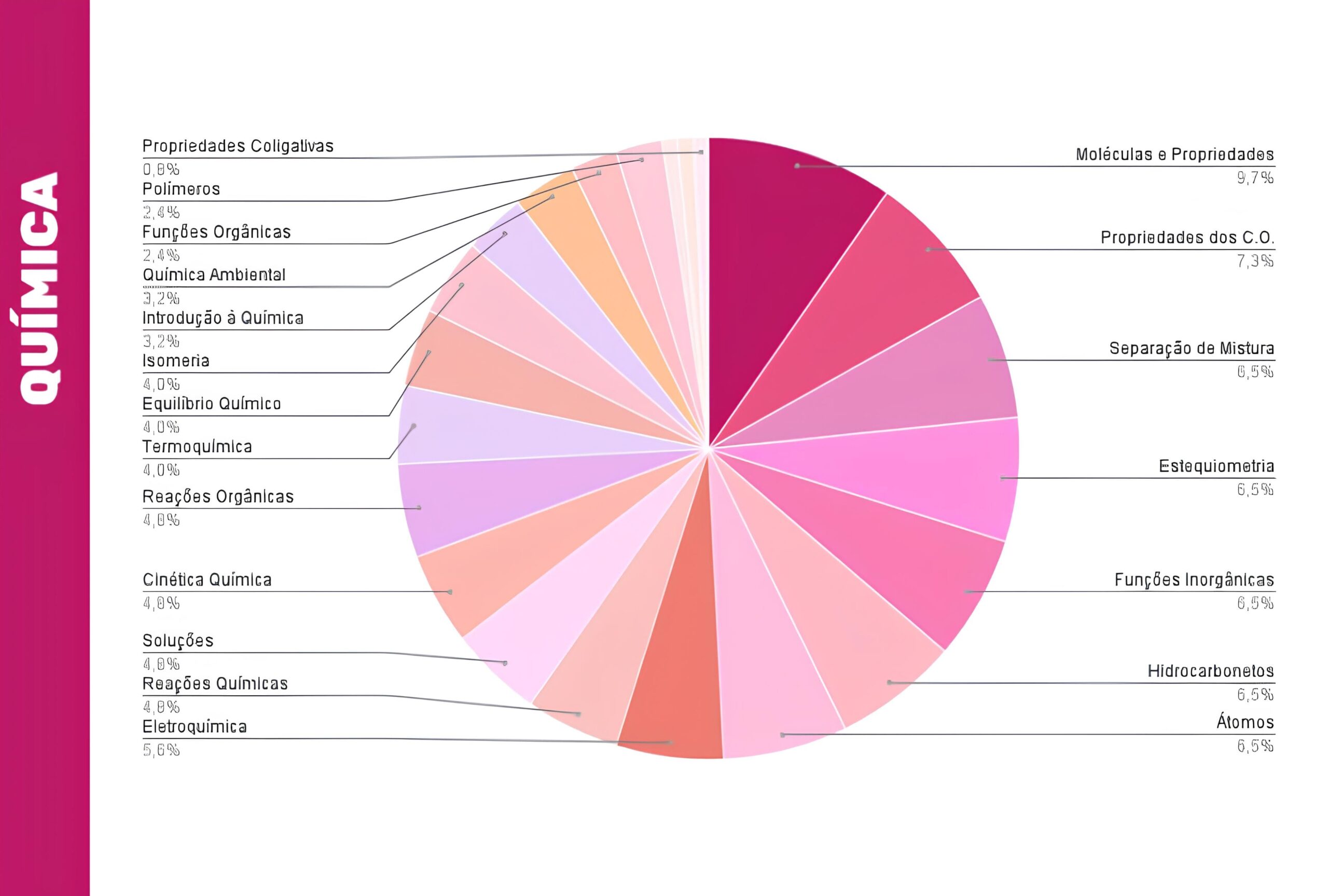
A prova do Enem, na disciplina de Química, costuma ser bem diversificada, abordando conteúdos introdutórios e mais aprofundados. Os que mais se destacam são:
- Moléculas e propriedades, com 9,7% de probabilidade de aparecer nas provas;
- Propriedades dos compostos orgânicos, com 7,3%;
- Separação de misturas, com 6,5%, assim como estequiometria, funções inorgânicas, hidrocarbonetos e átomos.
Continue lendo para aprender mais sobre essas temáticas e como elas aparecem no exame.
NAVEGUE PELOS CONTEÚDOS
1. Moléculas e propriedades
Este é o assunto que mais costuma marcar presença na prova de Química no Enem. O exame costuma trazer, em muitas questões, informações sobre as forças intermoleculares. Então, é de grande importância não apenas saber quais são as forças intermoleculares, mas também como funcionam nas interações entre moléculas.
E o segundo conteúdo que mais aparece, dentro desse assunto, é o NOX: Número de Oxidação. Nesse contexto, a prova traz a interpretação de reações, onde é necessário encontrar o nox dos elementos que a questão pede, nos reagentes e nos produtos.
⚠️ Importante sempre lembrar que, quando o elemento está sozinho, por exemplo “Cu(s)”, o nox é sempre 0.
Exemplo de questão sobre forças intermoleculares
(Enem 2019) A fluidez da membrana celular é caracterizada pela capacidade de movimento das moléculas componentes dessa estrutura. Os seres vivos mantêm essa propriedade de duas formas: controlando a temperatura e/ou alterando a composição lipídica da membrana. Neste último aspecto, o tamanho e o grau de insaturação das caudas hidrocarbônicas dos fosfolipídios, conforme representados na figura, influenciam significativamente a fluidez. Isso porque quanto maior for a magnitude das interações entre os fosfolipídios, menor será a fluidez da membrana.

Assim, existem bicamadas lipídicas com diferentes composições de fosfolipídios, como as mostradas de I a V.
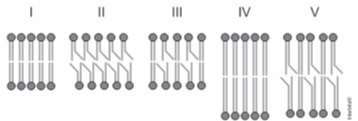
Qual das bicamadas lipídicas apresentadas possui maior fluidez?
a) I
b) II
c) III
d) IV
e) V
Resposta: [B]
De acordo com o texto, quanto maior for a magnitude das interações entre os fosfolipídios, menor será a fluidez da membrana. Invertendo o raciocínio: quanto menor for a magnitude das interações entre os fosfolipídios, maior será a fluidez da membrana.
Ao analisar as figuras, percebe-se que a insaturação diminui o contato entre as camadas. Por isso, quanto menor o contato (maior a quantidade de insaturações), maior será a fluidez e isto ocorre na figura II.
2. Propriedades dos compostos orgânicos
Dentre as propriedades dos compostos orgânicos mais cobradas, polaridade e pontos de fusão e ebulição saem na frente. É comum aparecerem moléculas orgânicas para que o candidato determine a qual delas pertence à descrição feita no comando da questão.
Polaridade dos compostos orgânicos
Aqui, é necessário conseguir identificar quando uma molécula orgânica é polar ou apolar, e qual será mais ou menos polar quando comparada à outras.
A dica é observar os heteroátomos (átomos diferentes de carbono e hidrogênio, como oxigênio, nitrogênio e enxofre.) presentes na cadeia - então, quanto mais heteroátomos, maior a polaridade da molécula orgânica.
Pontos de fusão e ebulição
Quanto aos pontos de fusão e ebulição, atente-se a três elementos: polaridade, massa e ramificação.
Moléculas de muita massa e lineares ou com poucas ramificações e polares têm maiores pontos de fusão e ebulição; enquanto moléculas menores, com mais ramificações e sem heteroátomos, têm menores pontos de fusão e ebulição.
Exemplo de questão sobre propriedades dos compostos orgânicos
(Enem 2023) O Aldrin é um inseticida agrícola organoclorado sintético de baixa polaridade, cuja estrutura molecular simétrica, de fórmula C12H8Cl6, está representada na figura. Introduzido na agricultura a partir da década de 1950, esse composto apresenta alta persistência no meio ambiente e acumulação nos organismos, sendo danoso para a saúde.
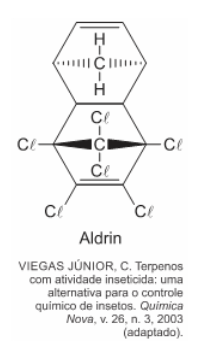
Um pesquisador coletou fluidos biológicos de indivíduos de uma população contaminada por esse inseticida agrícola. Ele analisou amostras de saliva, sangue, lágrima, urina e leite quanto à presença dessa substância.
Em qual dos fluidos o pesquisador provavelmente encontrou a maior concentração dessa substância?
a) Saliva, por consequência da atividade de enzimas.
b) Sangue, em função das hemácias e leucócitos.
c) Lágrima, em razão da concentração de sais.
d) Urina, pela presença de moléculas de ureia.
e) Leite, por causa do alto teor de gorduras.
Resposta: [E]
Conforme indicado no texto fornecido, Aldrin é um inseticida agrícola de baixa polaridade, pertencente à classe dos organoclorados sintéticos. Portanto, sua propensão é se dissolver em solventes apolares. Em resumo, a concentração mais elevada foi identificada no leite, devido ao seu elevado teor de gorduras predominantemente apolares.
3. Separação de misturas
O mais importante em separação de misturas é saber como separar tanto misturas heterogêneas, aquelas que apresentam mais de uma fase, quanto misturas homogêneas, aquelas que apresentam apenas uma fase.
Existem dois tipos de questões que aparecem com muita frequência em Química no Enem: uma delas dá a mistura de diferentes substâncias e pergunta sobre o método usado para separá-las; outra traz um processo industrial com diversas partes e indaga em qual delas ocorre uma separação de mistura específica.
A sacada é entender como são os processos de separação e identificar qual deles pode ser usado para separar cada mistura apresentada. Veja a seguir.
- sólidos: peneiração, catação, ventilação, magnetismo, levigação, fusão fracionada e dissolução fracionada;
- líquidos imiscíveis: o mais usado é o funil de separação;
- misturas de sólidos e líquidos: filtração, centrifugação, sedimentação, evaporação e filtração à vácuo;
- misturas homogêneas: destilação e extração.
Outro assunto que vem ganhando muito espaço em Química no Enem é o tratamento de água. É possível que a questão mostre uma estação de tratamento, com as etapas nomeadas, e pergunte em qual delas determinada separação de mistura acontece.
Exemplo de questão sobre separação de misturas
(Enem 2022) O urânio é empregado como fonte de energia em reatores nucleares. Para tanto, o seu mineral deve ser refinado, convertido a hexafluoreto de urânio e posteriormente enriquecido, para aumentar de 0,7% a 3% a abundância de um isótopo específico – o urânio-235. Uma das formas de enriquecimento utiliza a pequena diferença de massa entre os hexafluoretos de urânio-235 e de urânio-238 para separá-los por efusão, precedida pela vaporização. Esses vapores devem efundir repetidamente milhares de vezes através de barreiras porosas formadas por telas com grande número de pequenos orifícios. No entanto, devido à complexidade e à grande quantidade de energia envolvida, cientistas e engenheiros continuam a pesquisar procedimentos alternativos de enriquecimento.
ATKINS, P.; JONES, L. Princípios de química: questionando a vida moderna e o meio ambiente. Porto Alegre: Bookman, 2006 (adaptado).
Considerando a diferença de massa mencionada entre os dois isótopos, que tipo de procedimento alternativo ao da efusão pode ser empregado para tal finalidade?
a) Peneiração.
b) Centrifugação.
c) Extração por solvente.
d) Destilação fracionada.
e) Separação magnética.
Resposta: [B]
O procedimento alternativo ao da efusão seria a centrifugação dos hexafluoretos de urânio (UF6) gasosos formados pelos isótopos citados, pois suas massas são diferentes e, consequentemente, suas acelerações centrípetas.
👉 Leia também:
O que são misturas homogêneas e heterogêneas?
Tabela periódica: como ela surgiu e por que é tão importante?
4. Estequiometria
Na parte de estequiometria, a prova do Enem gosta sempre de trazer os cálculos estequiométricos, assim como os cálculos da massa atômica, molecular e molar, e também do rendimento das reações.
Então, se você achou que encontraria cálculos apenas em Matemática... A Química no Enem vai surpreender, pois essas questões são recheadas de cálculo! Existem perguntas, por exemplo, que pedem o cálculo da concentração percentual da substância, como veremos abaixo.
Exemplo de questão de estequiometria
(Enem 2023) Existe no comércio um produto antimofo constituído por uma embalagem com tampa perfurada contendo cloreto de cálcio anidro, CaCl2. Uma vez aberto o lacre, essa substância absorve a umidade ambiente, transformando-se em cloreto de cálcio di-hidratado, CaCl2 ⋅ 2 H2O.
Considere a massa molar da água igual a 18 g mol–1, e a massa molar do cloreto de cálcio anidro igual a 111 g mol–1.
Na hidratação da substância presente no antimofo, o ganho percentual, em massa, é mais próximo de
a) 14%
b) 16%
c) 24%
d) 32%
e) 75%
Resposta: [D]
\(1 \ CaCl_{2} + 2 \ H_{2}0 \rightarrow 1 \ CaCl_{2} \cdot 2 \ H_{2}O \)
\(111 \ g \ + \ \ \ 2 \ \cdot \ 18 \ g \ \ \ \ \ (111 + 2\cdot 18) \ g \)
\(111 \ g \ + \ \ \ \ \ \ 36 \ g \ \ \ \ \ \ \ \ \ \ \ \ \ \ \ 147 \ g \\ \)
\(111 \ g \ \rule{30 pt}{0.5 pt} \ 100 \% (anidro) \)
\(36 \ g \ \rule{30pt}{0.5 pt} \ p_{agua} \\ \)
\(p_{agua} \ = \frac {36 \ g \ \cdot 100 \%}{111 \ g} = 32,4324 \% \\ \)
\(p \cong 32% \)
5. Funções inorgânicas
No Enem, as funções inorgânicas podem aparecer em questões de diversas maneiras, incluindo:
- identificação das funções em reações químicas. Por exemplo, pode ser dado uma reação e a questão pede que identifique qual a função do composto X que reagiu com o composto Y. Ou como identificar um ácido, base, sal ou óxido em uma equação química.
- teorias ácidos-base, em que questões podem apresentar uma série de substâncias e solicitar a identificação de quais delas são ácidos, bases ou neutras, com base nos conceitos das diferentes teorias ácido-base, como a de Arrhenius, Brønsted-Lowry ou Lewis.
- identificação de doadores e receptores de prótons (na teoria de Brønsted-Lowry) ou pares de elétrons (na teoria de Lewis) na reação.
Exemplo de questão de funções inorgânicas
(Enem 2023) Em uma indústria, o controle da dureza da água é importante quando ela é utilizada em caldeiras, uma vez que sais pouco solúveis, formados a partir de sulfatos e carbonatos, podem acumular-se no interior das tubulações, causando obstruções. Para avaliar a água utilizada nessa indústria, foram realizados testes de qualidade que consideraram os seguintes parâmetros:
| Teste | Parâmetro medido |
|---|---|
| 1 | Cálcio |
| 2 | Cloreto |
| 3 | Turbidez |
| 4 | Coliformes totais |
| 5 | Sólidos sedimentáveis |
Qual teste deve ser considerado para controlar a formação desse tipo de obstrução de tubulações?
a) 1
b) 2
c) 3
d) 4
e) 5
Resposta: [A]
A presença elevada de íons cálcio e magnésio caracteriza a água dura. Portanto, é aconselhável realizar o teste 1, que consiste na medição da concentração de cálcio na água.
🥇 Quer preparação máxima para ter alto rendimento no Enem e ingressar no curso dos seus sonhos?
Então conheça a plataforma do Aprova Total!

Colaborou neste post: Júlia da Silva Cardoso



