Separação de misturas: métodos, exemplos e exercícios
Você já ouviu falar em separar óleo e água? Ou areia e ferro? Apresentamos métodos variados para separar misturas e quais as diferenças entre eles
Acessibilidade
A maioria dos materiais presentes na natureza não é uma substância pura, ou seja, constituída de um único tipo de partículas ou moléculas. Por isso, a separação de misturas é um processo importante para se ter conhecimento.
Você já ouviu falar em separar óleo e água? Ou areia e ferro? Não apenas por curiosidade, mas saber, por exemplo, como separar os poluentes das água e torná-la própria para consumo é essencial à vida na Terra.
Assunto interessante, né? Continue a leitura para conhecer quais são os métodos para separação de misturas homogêneas e heterogêneas, além de descobrir os detalhes de como isso é feito. Seguimos de olho no Exame Nacional do Ensino Médio (Enem) e nos vestibulares em geral.
NAVEGUE PELOS CONTEÚDOS
O que deve ser levado em consideração ao separar componentes de uma mistura?
Podemos dividir as misturas em homogêneas e heterogêneas. As misturas homogêneas têm mais de um componente presente, mas apresentam apenas uma fase. Um exemplo é a mistura entre sal e água: quando misturamos sal (NaCl) em um copo de água (H2O), temos apenas uma fase, mas há uma mistura de moléculas de água e íons Na+ e Cl-.
Assim, misturas homogêneas são formadas por dois ou mais componentes diferentes que se misturam entre si e formam, no fim, uma única fase.
Já as misturas heterogêneas têm componentes que não se misturam e ficam em fases diferentes. Um exemplo é a mistura entre água e o óleo: as duas substâncias não se misturam e, caso sejam colocadas em um copo, veremos o óleo na parte de cima e a água na parte de baixo.
Vale ressaltar que uma mistura heterogênea pode ter mais de duas fases. Esse número vai depender de quantos componentes que não se misturam estão presentes.
👉 Leia também:
O que estudar em Química para o Enem 2023
Ciências da Natureza: conheça 10 estratégias de estudo
Separação de misturas homogêneas
As misturas homogêneas necessitam de métodos especiais de separação, já que é mais difícil separá-las. Conheça quais são eles:
Destilação simples
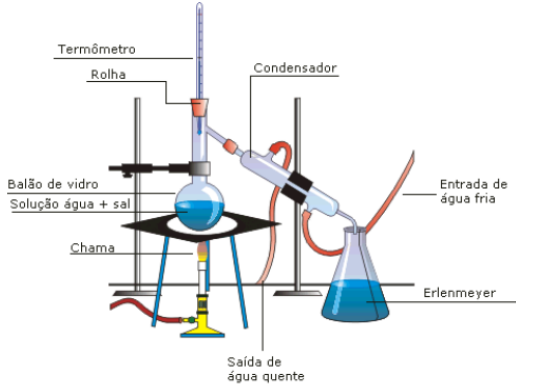
Nesse método, dissolvemos um soluto sólido em um solvente. Colocamos a solução em um balão de fundo redondo e aquecemos. Como o soluto tem um ponto de ebulição muito maior que o solvente, apenas o solvente irá evaporar, deixando o soluto no fundo do balão. O solvente atravessa um condensador e passa do estado de vapor para o líquido, sendo recolhido em um recipiente.
Dessa forma, no balão fica a substância com maior ponto de ebulição, enquanto a substância de menor ponto de ebulição evapora, para ser condensada e recolhida em outro recipiente. A dessalinização da água do mar é um exemplo:
Destilação fracionada
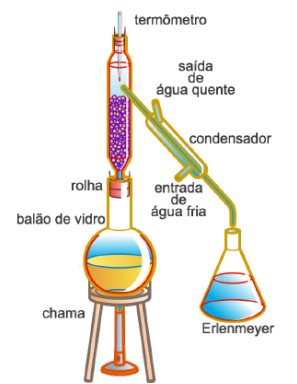
Usamos para separar misturas homogêneas que contêm líquidos com diferentes pontos de ebulição. Na destilação fracionada, colocamos a mistura em um balão de fundo redondo e aquecido. Então, o vapor das duas substâncias presentes na mistura sobe até uma coluna de destilação.
A substância com maior ponto de ebulição entra em contato com a coluna mais fria e condensa, caindo novamente no balão de fundo redondo. Já a substância com menor ponto de ebulição sobe até o topo da coluna, chegando a um condensador, onde finalmente volta a ser líquida e é recolhida em recipiente diferente.
A separação de componentes do petróleo é um exemplo. Ela ocorre em uma torre de destilação com "obstáculos" para a passagem do petróleo. A temperatura na base é maior que no topo, no intuito de impedir que os componentes mais pesados sejam evaporados com os mais leves:
Vaporização
Na vaporização, assim como da destilação simples, a mistura de um soluto sólido e de um solvente é aquecida. O solvente irá evaporar, enquanto o soluto permanecerá no recipiente. O que difere este método de separação da destilação simples é que não se recupera o solvente, pois ele evapora no ambiente. A roupa secando no varal é um exemplo.
Liquefação fracionada
Usamos esse método para separar misturas homogêneas de gases. A liquefação fracionada consiste em diminuir a temperatura ou aumentar a pressão até que os gases cheguem ao estado líquido. Em seguida, é feita a destilação fracionada da solução. Um exemplo é a separação do nitrogênio e do oxigênio presentes no ar atmosférico.
Fusão fracionada
Nesse método, conseguimos separar uma mistura homogênea de sólidos ao aquecer a mistura até que o componente com menor pondo de fusão se torne líquido, enquanto aquele com maior ponto de fusão permanece sólido. Temos como exemplo a separação do ferro e do chumbo.
Como o chumbo tem menor ponto de fusão (327,5 ºC) em relação ao ferro (1538 ºC), ele se muda para o estado líquido, enquanto o ferro permanece sólido.
Separação de misturas heterogêneas
Existe uma variedade imensa de métodos para separação de misturas heterogêneas, entre eles estão a filtração, a decantação, a centrifugação, a levigação e outros. Conheça mais sobre eles:
Filtração
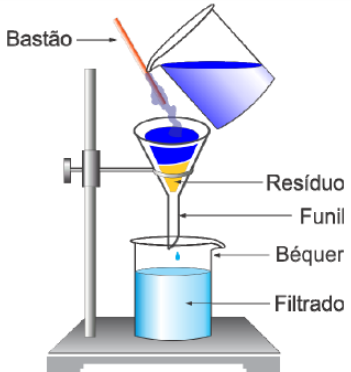
Serve para separar um sólido de um líquido. O sólido é barrado pelo filtro, enquanto o líquido não. Um exemplo é a separação de água e areia usando o filtro de café:
Decantação
O processo é ideal para separar um sólido de um líquido. Como o sólido não é solúvel no líquido, ele precipita, ou seja, vai para o fundo do recipiente. Então, fazemos a remoção do líquido sobrenadante da mistura sedimentada. Por exemplo, ao juntar água e areia, a mistura inicialmente fica com uma coloração turvam, mas, após um tempo, é possível realizar a separação:
Centrifugação
A centrifugação segue o mesmo princípio da decantação, porém, é uma forma de acelerar esse processo. Sendo assim, aplica-se uma força centrípeta para acelerar a separação dos componentes com densidades diferentes, em que a substância mais densa fica no fundo.
Separação magnética
Usa-se um imã para separar o material magnético de outro não magnético. Podemos, por exemplo, separar a areia (não magnética), da limalha de ferro (magnético), situação na qual a limalha será atraída para o imã.
Ventilação
Funciona de forma semelhante à levigação, porém, em vez de uma corrente de água, usamos a corrente de ar. Assim, o sólido menos denso é carregado pela corrente de ar, enquanto o mais denso continua no recipiente onde ocorre a separação da mistura. Exemplo: separar a casca e o grão de amendoim.
Flotação
A técnica consiste em adicionar ar a um meio para que as partículas em suspensão no líquido se aglutinem nas bolhas que aparecerem. Então, a espuma formada pode ser removida, levando com ela as partículas de impurezas. No caso de uma mistura com areia e serragem, ao adicionar água, a serragem vai flutuar e a areia afundar.
Levigação
Usamos a levigação para separar sólidos com diferentes densidades a partir das correntes de água. Neste método, o sólido menos denso é carregado pela corrente de água, enquanto o sólido mais denso fica no fundo do recipiente, realizando então a separação da mistura.

Floculação
Usamos bastante a floculação no tratamento de água, com o objetivo de agregar partículas coloidais. Para isso, adiciona-se um agente floculante à solução, fazendo com que essas partículas se agreguem. Isso é necessário porque as partículas, por conta de seu tamanho, não precipitam, além de passarem pelos poros dos filtros.
Após adicionar o agente floculante, as partículas se agregam em flocos, que decantam. Temos como exemplo a adição do sulfato de alumínio para aglutinar as partículas de impurezas (como barro, folhas, areia), formando os flocos.
Catação
Utiliza-se as mão ou algum instrumento, como pinças, para separar sólidos. Exemplo: separar as pedras dos grãos de feijão.
Adsorção
A adsorção ocorre quando partículas ficam retidas na superfície de um sólido. Podemos dividi-la em adsorção física e adsorção química. A primeira, que chamamos de fisissorção, ocorre quando as interações entre o sólido e as partículas adsorvidas são do tipo forças de Van da Walls; a outra, chamada quimissorção, ocorre durante uma reação química, que deixa a partícula adsorvida no sólido.
Temos como exemplo de adsorção o carvão ativado, que utilizamos para remover óleos, odores e muito mais, devido à sua estrutura com diversos poros que aumentam a retenção de substâncias.
Sifonação
Usamos para separar misturas sólidas e líquidas, ou líquidos que não se misturam. A sifonação consiste em colocar um cano no líquido que se deseja separar e, por diferença de pressão, o líquido escoa do recipiente mais alto para o mais abaixo. Exemplo: separar componentes de uma mistura de água e óleo.
Exercícios resolvidos sobre separação de misturas
Confira questões sobre separação de misturas que já caíram no Enem. O tema é o terceiro assunto mais cobrado na prova de Química, com 7,6% de incidência e destaque para tratamento de água, procedimentos experimentais e separação de misturas heterogêneas.
Exemplo 1
(Enem 2017) As centrífugas são equipamentos utilizados em laboratórios, clínicas e indústrias. Seu funcionamento faz uso da aceleração centrífuga obtida pela rotação de um recipiente e que serve para a separação de sólidos em suspensão em líquidos ou de líquidos misturados entre si.
RODITI. I. Dicionário Houaiss de física. Rio de Janeiro: Objetiva, 2005 (adaptado).
Nesse aparelho, a separação das substâncias ocorre em função
a) das diferentes densidades.
b) dos diferentes raios de rotação.
c) das diferentes velocidades angulares.
d) das diferentes quantidades de cada substância.
e) da diferente coesão molecular de cada substância.
Resposta: [A]
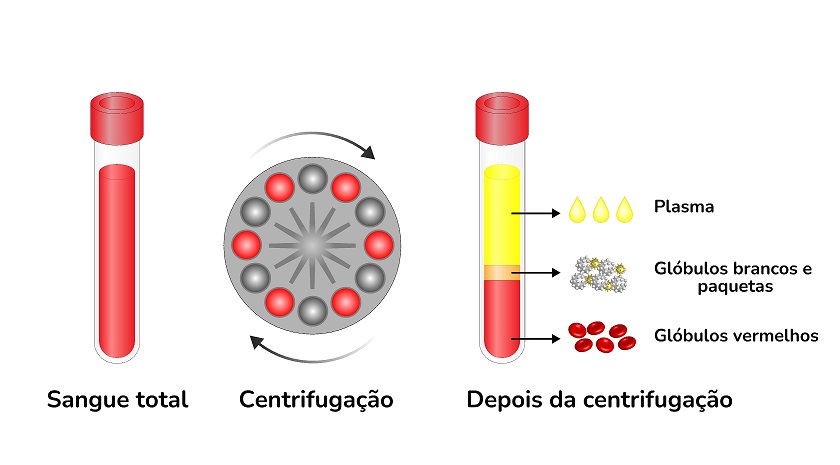
Nas centrífugas, a separação dos elementos de uma mistura acontece devido às discrepâncias em suas densidades e solubilidades. Temos como exemplo a centrifugação do sangue, onde ocorre a separação do plasma, células vermelhas e brancas.
Exemplo 2
(ENEM 2013) Entre as substâncias usadas para o tratamento de água está o sulfato de alumínio que, em meio alcalino, forma partículas em suspensão na água, às quais as impurezas presentes no meio aderem.
O método de separação comumente usado para retirar o sulfato de alumínio com as impurezas aderidas é a
a) flotação.
b) levigação.
c) ventilação.
d) peneiração.
e) centrifugação.
Resposta: [A]
Nas estações de tratamento de água destinada ao consumo da população, é necessário realizar diversas etapas para eliminar todos os poluentes presentes na água. Uma dessas etapas é a coagulação ou floculação, que envolve o uso de hidróxido de cálcio, conforme representado na seguinte reação:
3 Ca(OH)2 + Al2(SO4)3 → 2 Al(OH)3 + 3 CaSO4
O hidróxido de alumínio (Al(OH)3) resultante, sendo uma substância insolúvel em água, tem a capacidade de adsorver muitas das impurezas presentes na água, formando flocos. Para separar o sulfato de alumínio junto com as impurezas retidas, é comum utilizar o método de flotação. Esse processo envolve a agitação do sistema, fazendo com que as impurezas retidas subam à superfície da mistura heterogênea, onde podem ser facilmente removidas.




