Átomos: o que são e sua estrutura
Toda matéria que enxergamos é composta por átomos. Compreender esse assunto é fundamental para ter uma boa base na química

Acessibilidade
Tudo são átomos. Ou seja, toda a matéria que enxergamos (e a que não enxergamos) e que existe ao nosso redor é feita de átomos.
Por exemplo: imagine uma barra de ferro quebrando em mil pedaços. E cada pedacinho desses, se quebrando em mil pedaços novamente; e de novo, e de novo. Até que ponto esses pedaços podem ser quebrados e continuarem sendo Ferro?
Esse ponto é até chegarmos no átomo de ferro. Trilhões e trilhões e trilhões de átomos de ferro constituem uma peça de ferro tal qual conhecemos. Os gregos antigos, quando a ciência ainda era a filosofia, previram a existência do átomo. Para Leucipo e Demócrito, (300 a.C.), o átomo era uma partícula sólida, o menor constituinte da matéria que poderia existir. Esse foi o primeiro modelo atômico.
Dessa forma, hoje em dia, sabemos que o átomo não é a menor partícula que existe. Por isso, podemos "quebrar" o átomo em seus constituintes:
Núcleo: primeiramente temos o núcleo, onde está concentrada praticamente toda a massa do átomo. Ele é feito de prótons (partículas pesadas e positivamente carregadas) e nêutrons (partículas pesadas, sem carga nenhuma).
Eletrosfera: é a região próxima ao núcleo onde encontramos os elétrons, que podem ser entendidos como partículas de massa desprezível. Os elétrons possuem carga negativa e são atraídos pelo núcleo. Todas as reações e ligações químicas acontecem na região da eletrosfera, e não interferem no núcleo de um átomo.
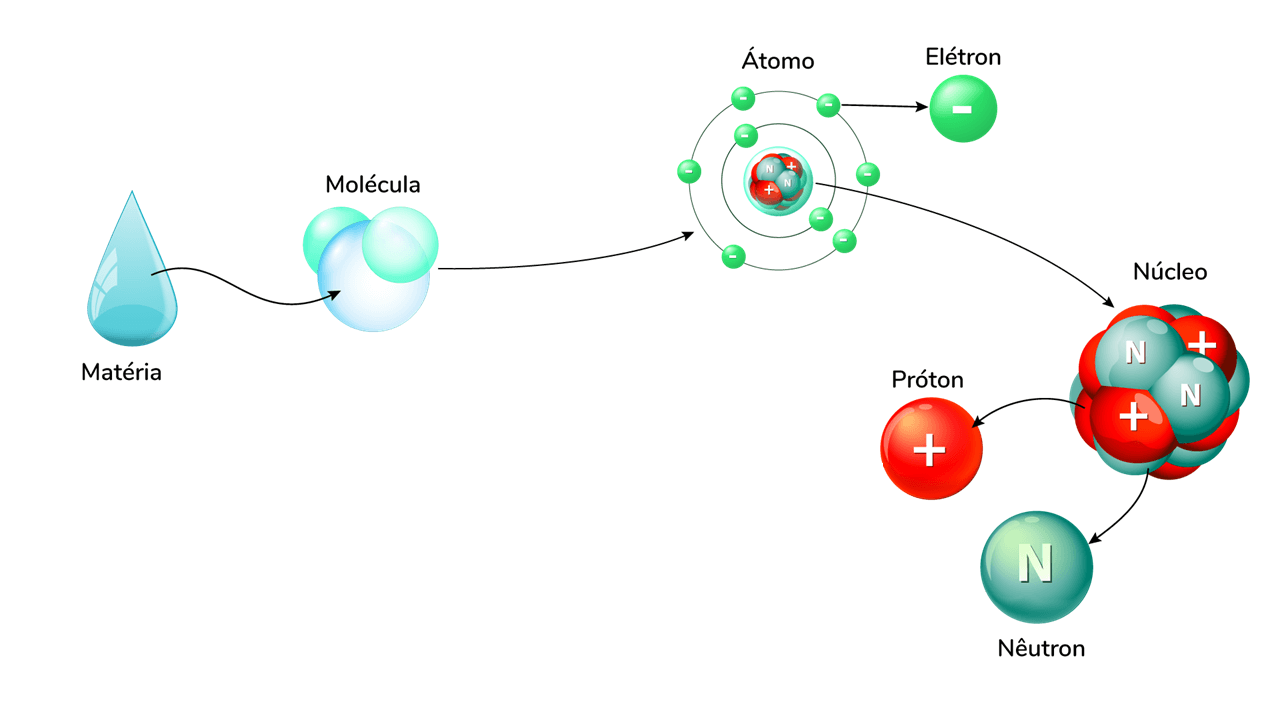
Aliás, a diferença de tamanho entre o núcleo do átomo e sua eletrosfera é tão grande que se o núcleo fosse do tamanho de uma bola de ping-pong, a órbita do elétron mais próximo seria do tamanho do Maracanã!
NAVEGUE PELOS CONTEÚDOS
Estrutura do átomo: partículas subatômicas
O átomo, então, é constituído por prótons, nêutrons e elétrons. Igualmente, cada um deles têm características próprias e é muito importante para as propriedades da matéria.
Nêutrons: estão presentes no núcleo do átomo. Eles têm massa, mas não tem carga.
Prótons: são partículas que possuem massa e carga positiva. Igualmente estão presentes no núcleo do átomo. Um elemento químico é caracterizado pelo número de prótons que um átomo possui. Por isso, saber a quantidade de prótons em um átomo é muito importante. Eventualmente é esse número que vai ditar as propriedades químicas de um átomo, quais reações ele sofrer, quais ligações químicas ele pode formar.
Elétrons: têm carga negativa. O número de elétrons (negativos) ao redor do núcleo é igual ao número de prótons (positivos). Por isso, os átomos são espécies neutras. Dessa forma, todas as reações químicas acontecem com os elétrons dos átomos, e não alteram o núcleo. O comportamento dos elétrons pode ser de partícula ou de onda, dependendo do ambiente.
Átomos e elementos químicos
Um elemento químico é uma classificação que criamos para enquadrar todos os átomos que possuem o mesmo número de prótons.
Por exemplo, uma barra de ferro é inteiramente constituída por átomos que contêm 26 prótons, que são os átomos do elemento químico ferro. Todos os átomos que existem no universo e possuem 26 prótons pertencerão ao elemento químico ferro.
O oxigênio que respiramos é constituído também por átomos - do elemento químico oxigênio. Esses, por sua vez, contêm apenas 8 prótons. Veja alguns exemplos:
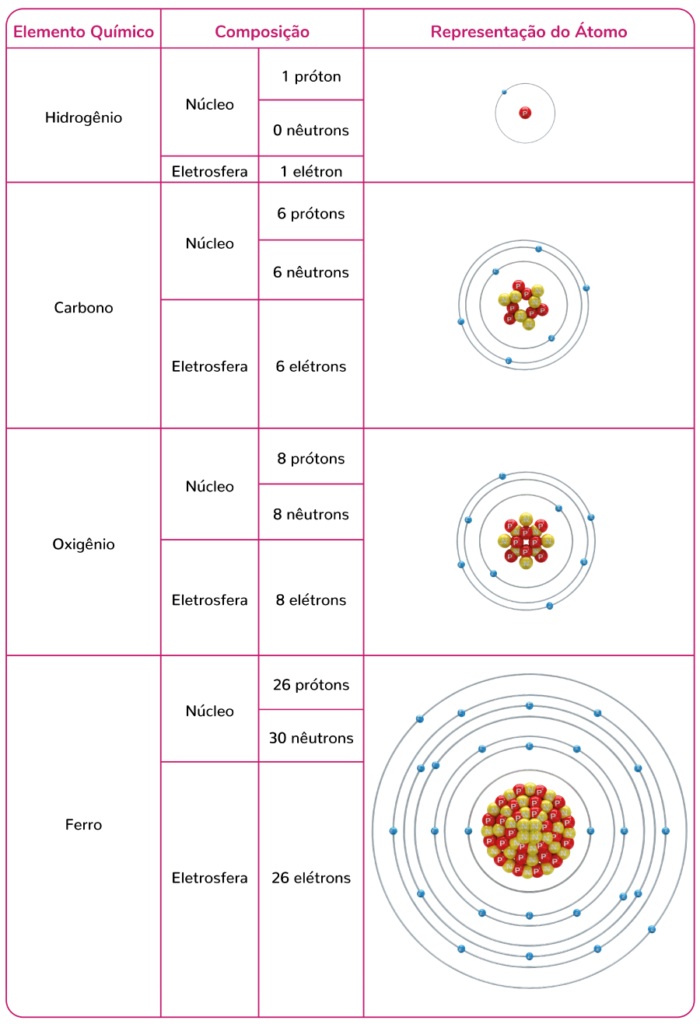
Veja que os elétrons estão organizados em camadas ao redor do núcleo. Como os elétrons são negativamente carregados, existe uma repulsão entre os elétrons, e uma atração pelo núcleo.
Assim, existe um número máximo de elétrons que cabe a determinada distância do núcleo (camada). Por exemplo, a camada mais próxima do núcleo só comporta dois elétrons.
| Camada | Quantidade de Elétrons |
| 1 | 2 |
| 2 | 8 |
| 3 | 18 |
| 4 | 32 |
Símbolos atômicos
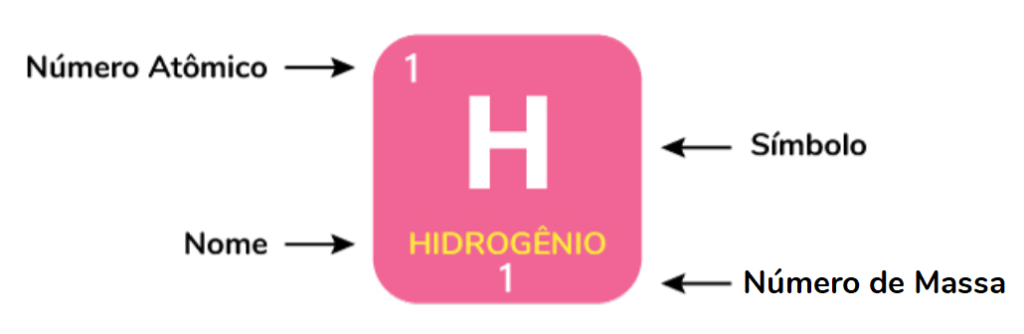
A cada tipo de átomo está associado a um símbolo que representa o elemento químico, um número atômico e um número de massa.
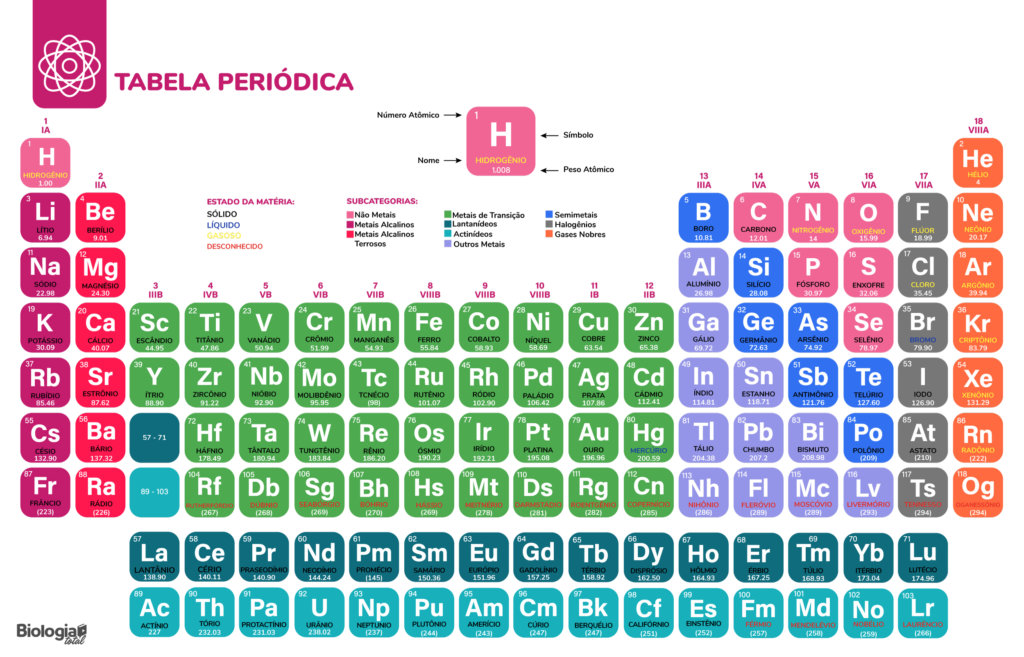
Símbolo: representa o elemento químico. Por exemplo o ferro pode ser representado por Fe, oxigênio, por O, e hidrogênio, H. Eles estão representados na tabela periódica dos elementos.
Número atômico (Z): é o número de prótons de um átomo.
Número de massa (A): é a soma do número de prótons e de nêutrons de um átomo (A = Z + N). O número de elétrons não conta, porque eles possuem massa desprezível.
Quer se preparar para o Enem e vestibulares com quem mais entende do assunto? A plataforma Aprova Total é a maior especialista no ensino digital e tem as melhores videoaulas e professores! Não deixe de conhecer os cursos Enem Hard e Super MED!




