Hidrocarbonetos: a função orgânica mais simples entre as substâncias
Eles são moléculas constituídas apenas de carbonos e hidrogênios, e estão presentes na maioria dos combustíveis minerais. Aprenda mais sobre os alcanos, alcenos, alcinos e compostos aromáticos neste post

Acessibilidade
Os hidrocarbonetos representam a função orgânica mais simples entre as substâncias, já que se constituem apenas de carbono e hidrogênio.
Eles estão presentes na maioria dos combustíveis minerais, por isso, compreender seus tipos, nomenclatura e propriedades é fundamental para estudantes que estão se preparando para o Exame Nacional do Ensino Médio (Enem) e os vestibular em geral.
A partir de agora, vamos explorar alcanos, alcenos, alcinos, cíclicos e hidrocarbonetos aromáticos, sempre com destaque para suas características e aplicações.
NAVEGUE PELOS CONTEÚDOS
O que são hidrocarbonetos?
Toda substância orgânica que se constitui apenas de hidrogênio e carbono classifica-se como um hidrocarboneto. Em sua maioria, os hidrocarbonetos são obtidos da destilação do petróleo, apesar de poucos serem encontrados naturalmente.
Os hidrocarbonetos estão muito presentes no nosso cotidiano.

Basta acender uma vela, abastecer o carro, ligar o fogão ou observar o amadurecimento dos alimentos que você os encontrará em abundância.
Características físico-químicas dos hidrocarbonetos
As características físico-químicas dos hidrocarbonetos variam dependendo do tipo de hidrocarboneto e da estrutura molecular específica. Essas propriedades podem variar dependendo da estrutura molecular específica de cada composto.
A seguir, listamos algumas dessas propriedades:
- Solubilidade: hidrocarbonetos são geralmente insolúveis em água pela natureza apolar das ligações carbono-carbono e carbono-hidrogênio. No entanto, eles são solúveis em solventes apolares, como outros hidrocarbonetos e solventes orgânicos.
- Ponto de fusão e ebulição: nos hidrocarbonetos, eles aumentam conforme a massa molar cresce. Alcanos de cadeia mais longa, por exemplo, tendem a ter pontos de fusão e ebulição mais altos em comparação com alcanos de cadeia mais curta.
- Densidade: varia de acordo com a estrutura molecular e a composição. Alcanos e hidrocarbonetos aromáticos, por exemplo, geralmente possuem densidades menores que a água, enquanto os alcenos e alcinos podem ter densidades maiores.
- Reatividade: alguns são mais reativos que outros devido à presença de ligações duplas (alcenos) ou triplas (alcinos) em suas estruturas. Essas ligações insaturadas tendem a ser mais reativas em reações químicas, como adições eletrofílicas.
- Inflamabilidade: muitos hidrocarbonetos são altamente inflamáveis. Isso ocorre por causa da presença de ligações carbono-hidrogênio, que se quebram facilmente em reações de combustão e liberam grandes quantidades de energia.
- Estabilidade: alcanos saturados são geralmente mais estáveis do que hidrocarbonetos insaturados (alcenos e alcinos), pela presença de ligações simples entre átomos de carbono. Hidrocarbonetos aromáticos também exibem uma estabilidade especial devido à ressonância do anel aromático.
Nomenclatura dos hidrocarbonetos
É preciso entender que existe uma lógica, ou seja, uma sistematização para atribuir o nome dos compostos orgânicos. O órgão responsável se chama IUPAC (União Internacional de Química Pura e Aplicada), assim, ao nomear um hidrocarboneto é necessário reconhecer o seu prefixo, infixo (afixo) e sufixo.
Na parte inicial do nome tem-se o prefixo, que estabelece a quantidade de carbonos presentes na cadeia carbônica. Toda vez que alterar a quantidade de carbonos presente na cadeia, seu prefixo será alterado.
Veja na tabela com exemplos de até 10 carbonos: a nomenclatura não se limita até o número 10, porém cadeias com mais de 10 carbonos são menos comuns.
| Prefixo | Nº de carbonos |
| met | 1 |
| et | 2 |
| prop | 3 |
| but | 4 |
| pent | 5 |
| hex | 6 |
| hept | 7 |
| oct | 8 |
| non | 9 |
| dec | 10 |
No centro do nome encontra-se o infixo (afixo), que é responsável pela indicação da presença ou ausência de insaturação, ou seja, tipo de ligação entre carbonos.
| Infixo | Ligação |
| an | Só ligações simples |
| en | 1 ligação dupla |
| adien | 2 ligações duplas |
| atrien | 3 ligações duplas |
| in | 1 ligação tripla |
| adiin | 2 ligações triplas |
| atriin | 3 ligações triplas |
Para finalizar a nomenclatura tem-se o sufixo, que é a terminação “o” no caso dos hidrocarbonetos. Quando se altera a função orgânica, o sufixo se altera também.
Para as cadeias insaturadas de hidrocarbonetos, como nos alcenos, nos alcinos e nos aromáticos, existe a possibilidade de localizar as ligações duplas ou triplas em carbonos distintos. Por isso, é necessário numerar a cadeia carbônica com os menores números inteiros possíveis. Veja o exemplo:
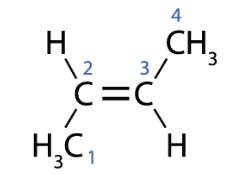
A partir da numeração dos carbonos, é possível notar que a ligação dupla está entre o carbono 2 e 3. Caso a contagem se inicie da esquerda para direita ou ao contrário, a insaturação estará no carbono 2. Nunca se esqueça de atribuir os menores números inteiros possíveis.
O nome para o composto orgânico será: But-2-eno.
Classificação dos hidrocarbonetos
Os hidrocarbonetos são classificados em diferentes grupos, cada um deles com suas especificidades. Vamos explorar os alcanos, alcenos, alcinos, cíclicos e hidrocarbonetos aromáticos, destacando as características de cada grupo.
Alcanos
Alcanos são os hidrocarbonetos saturados em que todos os carbonos fazem apenas ligações simples. Ou seja, só existe uma ligação covalente entre os carbonos.
Nos alcanos, todos os carbonos têm hibridização sp³, por isso, têm geometria tetraédrica. Sua fórmula geral é CnH2n+2.
Um exemplo mais conhecido de alcano é o metano: ele possui apenas um carbono em sua cadeia, que está realizando ligações simples com três átomos de hidrogênio.
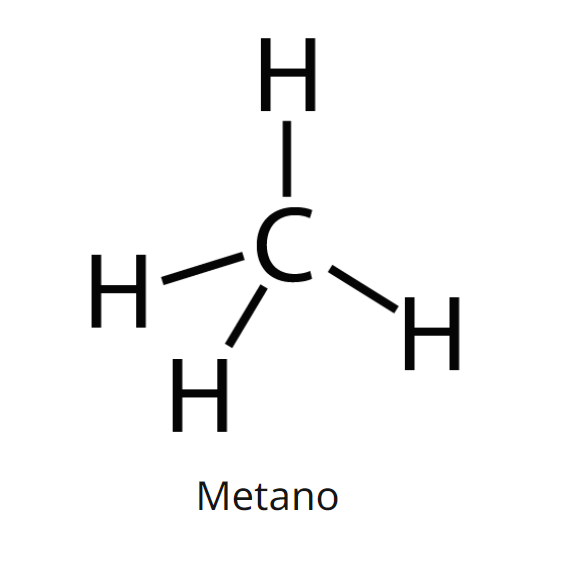
Alcenos
São os hidrocarbonetos em que existe pelo menos uma ligação dupla entre os átomos de carbono. Eles são insaturados porque os carbonos não fazem 4 ligações simples; ou seja, não estão ainda saturados de ligações simples.
Nos alcenos, há pelo menos dois carbonos com hibridização sp². Assim, fazem uma ligação sigma e outra pi, ficando fortemente ligados. Esses carbonos possuem geometria trigonal plana.
A fórmula geral dos alcenos é CnH2n. Um dos alcenos mais importantes é o eteno, que possui uma ligação dupla em sua cadeia entre os dois átomos de carbono.
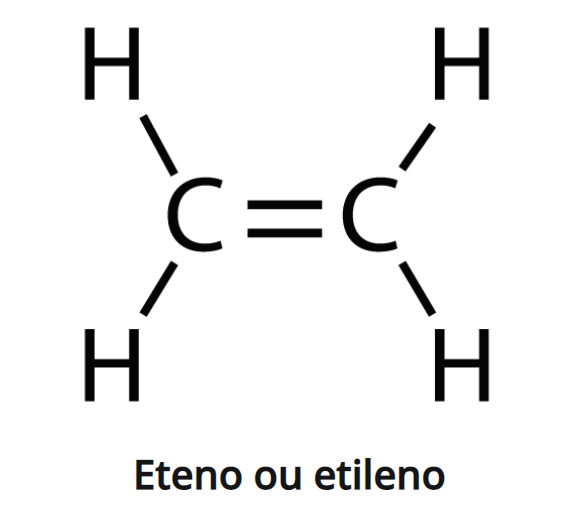
👉 Leia também:
Química no Enem 2024: veja os temas que mais aparecem na prova
13 fórmulas de Química que podem ajudar você no Enem
Tabela periódica: como ela surgiu e por que é tão importante?
Alcinos
Nesses hidrocarbonetos, existe pelo menos uma ligação tripla entre os átomos de carbono.
Tais carbonos possuem hibridização sp, por isso, têm geometria linear. Assim, entre esses carbonos existe uma ligação sigma e duas ligações pi. Então, eles estão fortemente ligados.
Os alcinos também são hidrocarbonetos insaturados. Como fazem duas ligações duplas, não estão saturados de ligações simples. Essas ligações pi, nas condições corretas, poderiam se romper para formar ligações simples com hidrogênios, saturando a molécula.
Sua fórmula geral é CnHn. O etino é um exemplo de alcino, gás utilizado como combustível industrial de maçaricos.

Cíclicos
Os hidrocarbonetos cíclicos são um grupo de compostos orgânicos que possuem pelo menos um anel de carbono em sua estrutura molecular. Os anéis podem conter uma variedade de ligações simples, duplas ou triplas entre os átomos de carbono, formando estruturas fechadas.
Esses compostos se caracterizam por sua estabilidade estrutural, devido à formação dos anéis, e podem exibir propriedades físicas e químicas únicas em comparação com hidrocarbonetos não cíclicos.
A estabilidade dos hidrocarbonetos cíclicos é influenciada pela conjugação de ligações duplas ou triplas, que pode gerar ressonância eletrônica dentro do anel, conferindo uma estabilidade adicional.
Alguns exemplos comuns de hidrocarbonetos cíclicos incluem:
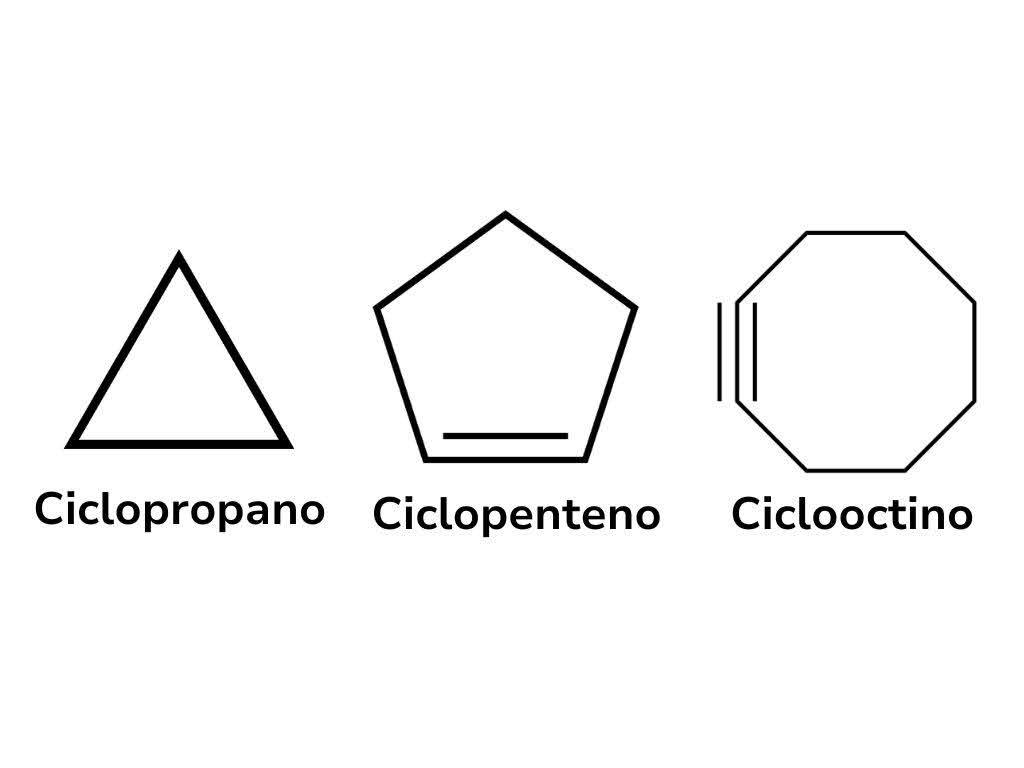
Cicloalcanos: hidrocarbonetos cíclicos saturados, ou seja, possuem apenas ligações simples entre os átomos de carbono no anel. Exemplo: ciclopropano.
Cicloalcenos: hidrocarbonetos cíclicos que contêm pelo menos uma ligação dupla entre átomos de carbono no anel. Exemplo: ciclopenteno.
Cicloalcinos: hidrocarbonetos cíclicos que contêm pelo menos uma ligação tripla entre átomos de carbono no anel. Exemplo: ciclooctino.
Hidrocarbonetos aromáticos
São os hidrocarbonetos cíclicos, que possuem ligações duplas alternadas, conhecidos como anéis aromáticos.
Eles não possuem fórmula geral, mas nos vestibulares, costumam aparecer apenas como derivados do benzeno.
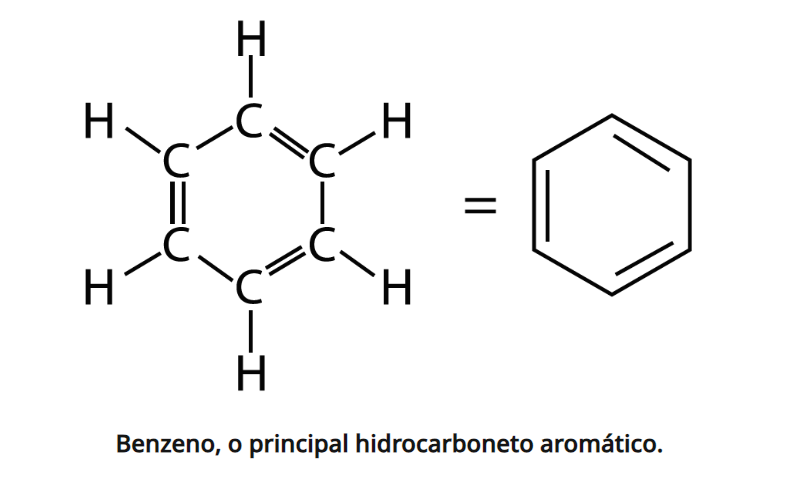
Por terem ligações duplas alternadas, nos anéis aromáticos todos os carbonos têm hibridização sp², de geometria trigonal plana. Assim, cada carbono faz duas ligações sigma e uma pi com outro carbono.
Isso dá aos aromáticos uma propriedade muito especial, a ressonância dos elétrons pi. Esses elétrons das ligações pi são compartilhados com todos os carbonos da molécula; não ficam localizados somente entre dois carbonos.
Propriedades gerais dos hidrocarbonetos
Por se parecerem bastante, essa função orgânica tem propriedades químicas e físicas muito semelhantes, a variar pela cadeia carbônica.
Em geral, obrigatoriamente todos os hidrocarbonetos são apolares. Sendo assim, são completamente insolúveis em água.
Assim, quando ocorrem os vazamentos de petróleo, substância constituída integralmente de hidrocarbonetos, o impacto ambiental é catastrófico por conta de suas propriedades físicas.
🦆 No caso das aves, que possuem ceras em suas penas, o petróleo é especialmente danoso, pois, devido à sua apolaridade, ele se espalha pelos corpos e fica aderido nas penas.
O estado físico de cada hidrocarboneto está relacionado ao tamanho de suas cadeias carbônicas e como elas interagem entre si, sendo a força das interações uma consequência do grau de insaturação e do número de substituintes.
Considerando cadeias não ramificadas, que possuem somente carbonos primários e secundários, podemos generalizar da seguinte maneira:
- Hidrocarbonetos sólidos: cadeias com 18 ou mais carbonos
- Hidrocarbonetos líquidos: cadeias com 5 a 17 carbonos
- Hidrocarbonetos gasosos: cadeias com 1 a 4 carbonos
Quais são as principais aplicações dos hidrocarbonetos?
Os hidrocarbonetos possuem diversas funções na área da ciência. Alguma das principais são:
- Fonte de energia ou combustíveis: produtos como gasolina, diesel, querosene e gás natural são amplamente servem de combustíveis em veículos, motores industriais, sistemas de aquecimento residencial e na produção de eletricidade.
- Matéria-prima: diversos produtos químicos e materiais têm sua origem nos hidrocarbonetos. O petróleo bruto, uma complexa mistura desses compostos, é refinado para gerar plásticos, borrachas, solventes, lubrificantes, asfalto, fármacos e mais.
- Materiais sintéticos: hidrocarbonetos são fundamentais na produção de sintéticos como polietileno, polipropileno, poliestireno e PVC. Esses materiais encontram aplicação em diversos setores, como embalagens, construção, eletrônicos e têxteis.
- Síntese orgânica: por meio do hidrocarbonetos, uma ampla gama de compostos orgânicos é produzida, incluindo medicamentos, pesticidas, fertilizantes, corantes, detergentes e cosméticos.
- Reagentes em química: alguns hidrocarbonetos participam como reagentes em diversas reações químicas orgânicas. Por exemplo, o etileno é comumente utilizado como matéria-prima na síntese de outros compostos orgânicos na indústria química.
- Solventes: usados em processos industriais e na fabricação de produtos de consumo, como tintas, vernizes, adesivos e produtos de limpeza.
Resumo: hidrocarbonetos
Os hidrocarbonetos, por sua simplicidade estrutural e diversidade, desempenham papel essencial na química orgânica. Vamos retomar os principais pontos abordados neste artigo?
- Os hidrocarbonetos são compostos químicos que se constituem de átomos de hidrogênio e carbono;
- Eles são a base dos combustíveis fósseis, como petróleo, gás natural e carvão mineral;
- Classificam-se em dois grupos principais: alifáticos (cadeias abertas) e aromáticos (anéis de carbono);
- Entre suas principais características estão baixa polaridade, inflamabilidade e solubilidade;
- São divididos entre alcanos (hidrocarbonetos saturados), alcenos (hidrocarbonetos insaturados), alcinos (hidrocarbonetos insaturados) e hidrocarbonetos aromáticos (contêm anéis de carbono ligados por ligações duplas alternadas);
- Entre as aplicações dos hidrocarbonetos para o dia a dia estão a produção de combustíveis; plásticos e polímeros; produtos químicos como solventes, lubrificantes e cosméticos; agroquímicos e medicamentos.

Como os hidrocarbonetos caem no Enem e vestibulares?
Tanto em vestibulares como no Exame Nacional do Ensino Médio (Enem), o conteúdo que costuma aparecer sobre os hidrocarbonetos envolve combustíveis e petróleo.
Confira alguns exemplos:
Exemplo 1
(UNICAMP 2017) “Pode arredondar?” Esta é uma pergunta que frentistas de postos de combustíveis fazem durante o abastecimento, quando o travamento automático da bomba é acionado. O fabricante do veículo faz a recomendação de não arredondar, pensando na preservação do veículo, mas o dono do posto pede que o frentista arredonde, para vender mais combustível. Por outro lado, pensando na saúde do frentista, prejudicada pela exposição aos vapores de combustível, pode-se afirmar corretamente que:
a) qualquer que seja a resposta do consumidor, até o travamento automático ou passando do automático, a saúde do frentista será prejudicada, pois sempre haverá eliminação de vapores durante o abastecimento.
b) a resposta mais adequada do consumidor seria “sim”, porque a quantidade de vapores eliminados no abastecimento é a mesma, e o prejuízo à saúde do frentista é o mesmo, independentemente do volume de combustível adicionado ao tanque.
c) a resposta mais adequada do consumidor seria “não”, pois somente a partir do travamento automático é que há eliminação de vapores durante o abastecimento e só depois disso há prejuízo para a saúde do frentista.
d) a resposta mais adequada do consumidor seria “sim”, porque não haverá eliminação de vapores durante o abastecimento e assim nunca haverá prejuízo para a saúde do frentista.
Resposta: [A]
Como os vapores liberados pelos combustíveis são tóxicos, qualquer que seja a resposta do consumidor, até o travamento automático ou passando do automático, a saúde do frentista será prejudicada, pois sempre haverá eliminação de vapores durante o abastecimento.
Exemplo 2
(Enem 2023) A gasolina é uma mistura de hidrocarbonetos de cadeias saturadas contendo de 8 a 12 átomos de carbono. Além disso, a gasolina de alto desempenho deve conter elevados teores de hidrocarbonetos de cadeias ramificadas, de forma a resistir à compressão e entrar em ignição apenas quando a vela aciona uma centelha elétrica no motor. No quadro, estão apresentados compostos que podem ser utilizados como combustíveis.
| Composto | Nomenclatura |
| I | n-decano |
| II | n-heptano |
| III | 2,2,4-trimetilpentano |
| IV | 3-etil-4-metilex-1-eno |
| V | 3-etil-2-metilpentan-1-ol |
Entre esses compostos, aquele que conferirá maior desempenho como combustível é o
a) I.
b) II.
c) III.
d) IV.
e) V.
Resposta: [C]
Conforme mencionado no enunciado, a gasolina de alto desempenho necessita incluir quantidades substanciais de hidrocarbonetos de cadeias ramificadas, especificamente carbonos terciários e/ou quaternários. Isso é crucial para resistir à compressão e iniciar a ignição somente quando a vela elétrica no motor é acionada. O composto III exibe essas características.
