Isomeria Plana: tipos, funções, características e mais
Do grego, isos = igual e meros = partes; isto é, podem existir compostos de mesma
fórmula molecular, mas com propriedades físicas e químicas únicas. Entenda a isomeria plana nesse blog post!

Acessibilidade
A isomeria plana é uma área da química orgânica que estuda a isomeria entre moléculas através de suas fórmulas estruturais planas. Ou seja, aquela em que a organização espacial dos átomos não é relevante, diferente da isomeria óptica.
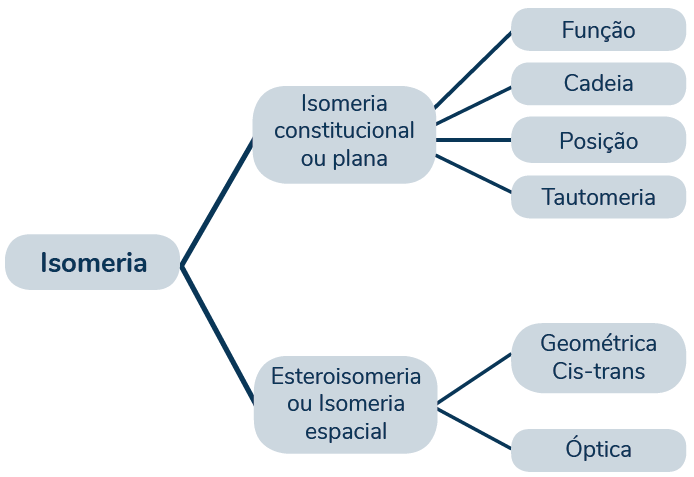
Assim, a isomeria plana ou constitucional, pode ser dividida em quatro tipos: isomerias de função, de cadeia, de posição e a tautomeria.
É importante lembrar que um par de isômeros são moléculas cujas fórmulas moleculares são exatamente as mesmas, mas a posição dos átomos em relação um ao outro é que muda.
Por exemplo, com a fórmula C3H8O, onde podemos montar um éter um álcool.
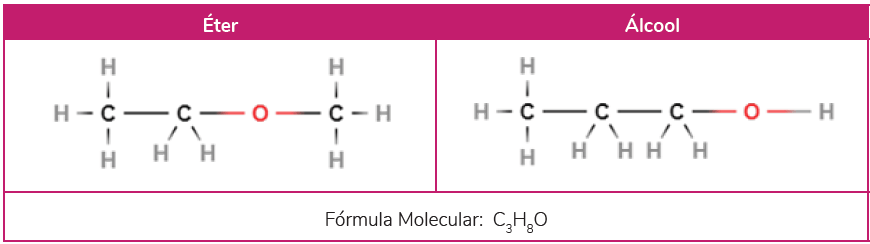
Assim, essas moléculas são isômeras: possuem mesma fórmula molecular, mas propriedades físicas e químicas diferentes, por causa das diferentes ligações químicas que cada átomo realiza.
NAVEGUE PELOS CONTEÚDOS
Tipos de isomeria plana
De função
A isomeria de função é exatamente aquela mostrada no exemplo anterior. São moléculas que possuem a mesma fórmula molecular, mas pertencem à funções orgânicas diferentes.
Dessa forma, as propriedades físicas e químicas desses isômeros são bastante diferentes. Assim como as reações químicas que participam, ponto de fusão e ebulição são completamente diferentes, apesar de possuírem a mesma fórmula e massa molecular.
Veja os exemplos:
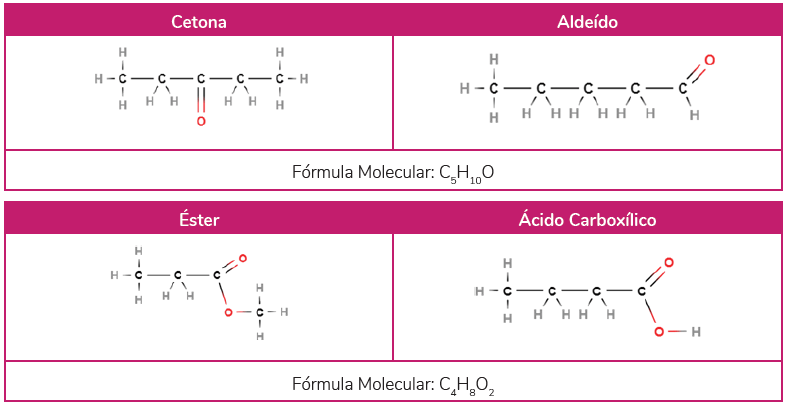
De cadeia
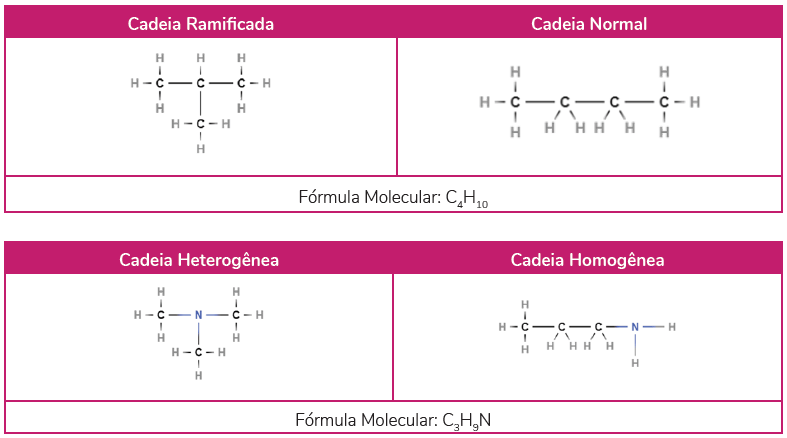
Ela acontece quando dois isômeros, que pertencem à mesma função química, possuem também a mesma fórmula molecular, mas sua cadeia carbônica é diferente. Nesse caso, devemos nos atentar às alterações na cadeia principal.
A cadeia carbônica pode variar em ramificação, grau de saturação, ser aberta ou fechada, homogênea ou heterogênea... Enfim, todas as variações que se pode construir mantendo a mesma fórmula molecular.
Veja alguns exemplos:
De posição
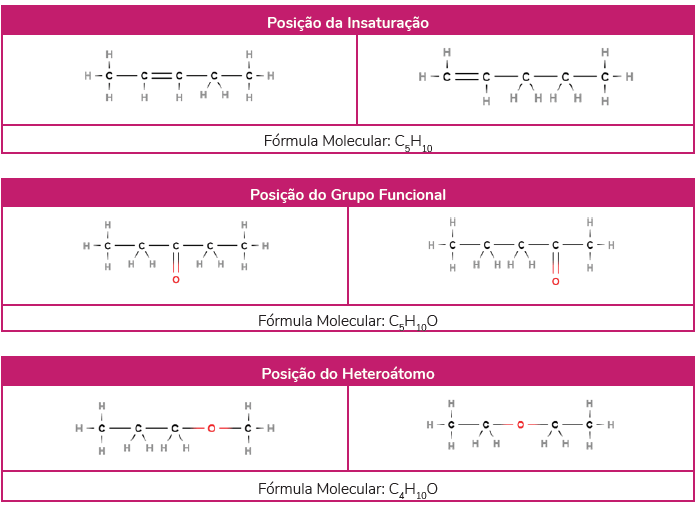
Quando o que difere entre um grupo de moléculas em análise é a posição da insaturação, do grupo funcional, do heteroátomo ou da ramificação, dizemos que a ela é de posição.
Nesse tipo de isomeria, as moléculas pertencem à mesma função orgânica. Por exemplo, cetonas e aldeídos com o mesmo número de carbonos costumam ser isômeros entre si; porém, essa isomeria é de função. Se apenas realocarmos a posição da carbonila de uma cetona (C=O), mantendo-a entre carbonos, continuaremos com uma cetona - essa é a isomeria de posição. Se trocarmos a posição da carbonila para uma das extremidades, teremos um aldeído, e portanto, será isomeria de função.
E claro, as propriedades da substância são alteradas quando se altera alguma coisa em sua estrutura, nunca se esqueça!
Isomeria plana de compensação ou tautomeria
A isomeria de compensação, tautomeria, ou isomeria constitucional dinâmica é chamada assim devido ao equilíbrio estabelecido em solução aquosa entre compostos com mesma fórmula molecular e função química diferente.
Mesmo sendo de função, porém, ela não é estática! Como assim?
Não se tratam de duas moléculas diferentes, mas sim uma mesma molécula que estabelece um equilíbrio entre duas funções químicas distintas: ela "troca" de função constantemente quando em meio aquoso.
Existem apenas dois grupos: Tautomeria aldo-enólica e Tautomeria Ceto-enólica.
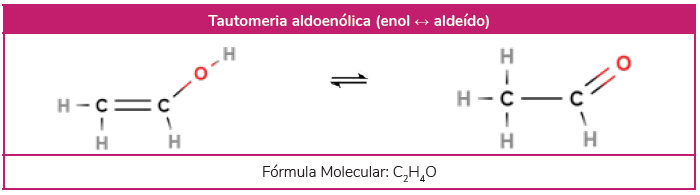
Nessa primeira, existe um equilíbrio entre um enol – molécula cujo grupo funcional -OH está ligado a um carbono sp² -, e um aldeído. Esse equilíbrio é dinâmico e acontece porque a ligação dupla dos enóis é instável.
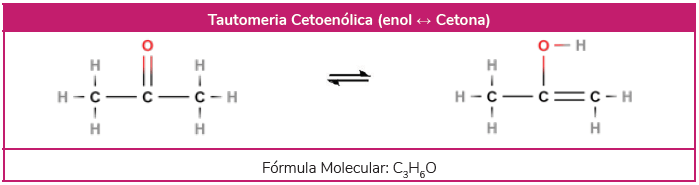
Na tautomeria ceto-enólica, uma cetona pode ser convertida a um enol, quando o oxigênio da cetona captura um hidrogênio de um carbono. Assim, a ligação C-H se desfaz e uma ligação O-H é formada. A dupla é transferida da ligação C=O para a ligação C-C.
🥇 Quer se preparar para o Enem e vestibulares com quem mais entende do assunto? A plataforma Aprova Total é a maior especialista no ensino digital e tem as melhores videoaulas e professores!